2019 年諾貝爾生理學或醫學獎於北京時間 10 月 7 日下午 5 點 30
分公布,今年的獲獎者有三位,他們分別是來自哈佛醫學院達納-法伯癌症研究所的威廉·凱林( William G. Kaelin,
Jr.),牛津大學和弗朗西斯·克裏克研究所的彼得·拉特克利夫( Peter J. Ratcliffe)
以及美國約翰霍普金斯大學醫學院的格雷格·塞門紮(Gregg L. Semenza)。
他們因在氧感知通路方麵的研究做出的貢獻而獲獎。以下是丁香園編譯自諾貝爾獎官方網站上,對於幾位科學家研究成果的介紹。
動物需要氧氣才能將食物轉化為有用的能量。幾個世紀以來,人們致力於研究氧氣對於機體的重要性,但人們一直搞不清楚細胞如何適應氧氣水平的變化。
William G. Kaelin、Sir Peter J. Ratcliffe 和 Gregg L.
Semenza,他們發現了可以調節基因活性以應對不同氧氣濃度變化的分子機製。
今年諾貝爾獎獲得者開創性的發現,揭示了生命中最重要的適應過程之一的機製。他們為我們了解氧氣水平如何影響細胞代謝和生理功能奠定了基礎。
他們的發現也為治療貧血、癌症和許多其他疾病的新方法奠定了基礎。
氧氣:初登舞台
氧氣約占地球大氣層的五分之一,對動物生命至關重要:幾乎所有動物細胞中的線粒體都會利用氧氣,將食物轉化為有用的能量。
Otto Warburg 是 1931 年諾貝爾生理學或醫學獎的獲得者,他揭示了這種轉換是有酶參與促進的過程。
機體逐漸進化出確保向組織和細胞充分供氧的機製。頸動脈體與頸部兩側的大血管相鄰,包含了專門感應血液中氧氣水平的細胞。1938
年,Corneille Heymans
獲得的諾貝爾生理學或醫學獎,就是獎勵他發現了頸動脈體和主動脈體感知血氧水平並通過神經中樞調節呼吸頻率的作用。
HIF:進入視野
除了頸動脈體可以應對低氧水平(低氧)進行快速調節外,還有其他一些基本的生理適應性。對缺氧的主要生理反應是促紅細胞生成素(EPO)水平的升高,這會刺激紅細胞生成。激素控製紅細胞生成的重要性,在
20 世紀初就已為人所知,但是這種過程如何由氧氣濃度控製,仍然是個謎。
Gregg Semenza 研究了 EPO 基因,以及如何根據氧氣濃度來調節它。通過使用基因修飾的小鼠,顯示位於 EPO
基因旁邊的特定 DNA 片段介導了細胞對缺氧的反應。Sir Peter Ratcliffe 還研究了 EPO
基因的氧氣依賴性調節。
兩個研究小組都發現,幾乎所有組織中都存在氧傳感機製,而不僅存在於通常產生 EPO
的腎細胞中。這些重要發現表明,該機製在許多不同的細胞類型中是通用的,而且都具有作用。
Semenza
希望確定介導這種反應的細胞成分。在培養的肝細胞中,他發現了一種蛋白質複合物,該複合物以一種氧依賴性的方式與已鑒定出的 DNA
片段結合。他稱這種複合物為缺氧誘導因子(HIF)。
1995 年他開始了純化 HIF 複合物的工作,隨後 Semenza 發表了部分關鍵研究結果,其中包括明確 HIF 編碼基因、發現
HIF 由兩種不同的 DNA 結合蛋白組成(即所謂的轉錄因子,現在稱為 HIF-1α 和 ARNT)。現在,研究人員開始著手研究
HIF 的其他成分以及運作機製。
VHL:意想不到的夥伴
當機體裏的氧濃度很高時,細胞中幾乎不含 HIF-1α,當機體氧濃度偏低時,HIF-1α 的含量升高,這意味著它可以結合並調節
EPO 基因以及其他具有 HIF 結合 DNA 片段的基因。
2004 年諾貝爾化學獎得主 Aaron Ciechanover,Avram Hershko 和 Irwin Rose
發現,在正常的氧氣水平下,一種小肽泛素被添加到 HIF-1α 蛋白中,這種泛素標記使得 HIF-1α 在蛋白酶體中被降解。
此外,幾個研究小組都表明,在缺氧條件下,原本被迅速降解的 HIF-1α 通常不會被繼續降解。 然而,泛素如何以氧依賴性方式結合
HIF-1α 仍然是一個關鍵問題。
答案來自一個意想不到的方向。
Ratcliffe 與 Semenza 大約同時在探索 EPO 基因的調控,癌症研究者 William Kaelin,Jr.
正在研究一種遺傳綜合征,即 von Hippel-Lindau 病(VHL 病)。這種遺傳疾病會導致遺傳性 VHL
突變的家庭罹患某些癌症的風險急劇增加。
Kaelin 的研究結果表明,VHL 基因可以編碼產生具有預防癌症發生作用的蛋白質。此外,缺乏功能性 VHL
基因的癌細胞會異常高水平表達低氧調節基因,但是將 VHL 基因重新引入癌細胞後,低氧調節基因表達可恢複正常水平。
這是一個重要的線索,表明 VHL 以某種方式參與了對缺氧反應的控製。
來自幾個研究小組的其他線索表明,VHL
是複合物的一部分。該複合物用泛素標記蛋白質,被泛素標記的蛋白質隨後被蛋白酶體降解。Ratcliffe
及其研究小組隨後有一個關鍵發現:他們證明了機體在正常氧濃度下降解 VHL需要通過 VHL 與 HIF-1α
發生物理相互作用實現,這最終將 VHL 與 HIF-1α 聯係到了一起。
氧氣感應機製及其工作原理
許多研究結果都已經就位,但是仍然缺少對氧氣水平如何調節 VHL 和 HIF-1α 之間相互作用的理解。研究的重點區域在已知對
VHL 降解具有重要作用的 HIF-1α 蛋白的特定部分,Kaelin 和 Ratcliffe
都懷疑氧氣感測的關鍵位於該蛋白結構域的某個位置。
在 2001 年,他們在兩篇同時發表的文章中表明,在正常的氧氣水平下,HIF-1α
蛋白的兩個特定位置會添加羥基。這種蛋白質修飾(稱為脯氨酰羥化)使 VHL 能夠識別並結合到
HIF-1α,從而解釋了正常的氧氣水平如何通過對氧敏感的酶(所謂的脯氨酰羥化酶)來控製 HIF-1α 的快速降解。
Ratcliffe 等人的研究,進一步確定了特定的脯氨酰羥化酶,並表明 HIF-1α
的基因激活功能受氧氣依賴性羥基化作用的調節。至此,三位諾貝爾獎獲得者,已經闡明了氧氣感應機製,並展示了其工作原理。
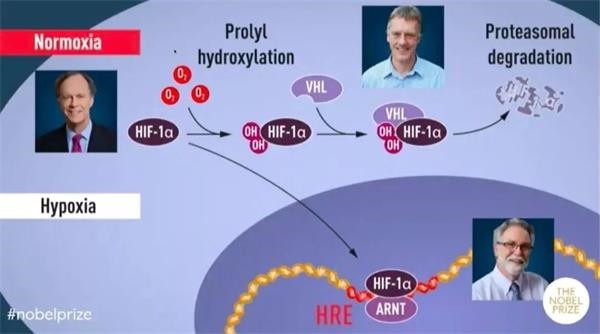
當氧水平低(低氧)時,HIF-1α 被保護免於降解,積聚在細胞核中,與 ARNT 及低氧調節基因中的特定 DNA
序列(HRE)結合(1)。在正常的氧氣水平下,HIF-1α 被蛋白酶體迅速降解(2)。氧氣通過向 HIF-1α
添加羥基(OH)來調節降解過程(3)。隨後,VHL 蛋白可以識別 HIF-1α
並與之形成複合物,從而導致其以氧依賴性方式降解(4)。
氧氣影響的生理和病理
由於這些諾貝爾獎獲得者開創性的工作,我們對不同的氧氣水平如何調節基本的生理過程有了更多的了解。氧感知通路使細胞能夠進行新陳代謝,適應低氧水平:如劇烈運動期間的肌肉中。
與氧感知通路相關的其他適應性過程還包括,新血管的產生和紅細胞的產生。我們的免疫係統和許多其他生理功能也可以通過氧感知通路進行微調。此外,在胎兒發育過程中,氧感知通路對控製正常的血管形成和胎盤發育,已被證明是必不可少的。
氧感知通路也是許多疾病發生的核心。例如,由於EPO
由腎髒中的細胞產生,對於控製紅細胞的形成至關重要,所以慢性腎功能衰竭的患者,通常由於 EPO 表達降低而患有嚴重的貧血。
此外,氧調節機製在腫瘤發生過程中具有重要作用,利用氧氣調節機製刺激血管形成並重塑新陳代謝,可以使癌細胞有效增殖。
在學術實驗室和製藥公司中也在進行一些重要的研究,其中就包括研發可以通過激活或阻斷氧氣感應機製,來幹擾不同疾病狀態的藥物。
獲獎的氧感應機製在生理學中的新陳代謝、免疫反應和適應運動等都具有極其重要等作用。此外,許多病理過程也會受到影響。許多研究室與製藥公司正在不斷努力開發可以抑製或激活氧調節機製的新藥,以治療貧血,癌症和其他疾病。
華客網:一文幫你看懂今年諾獎成果 什麽是氧感知通路?(圖)